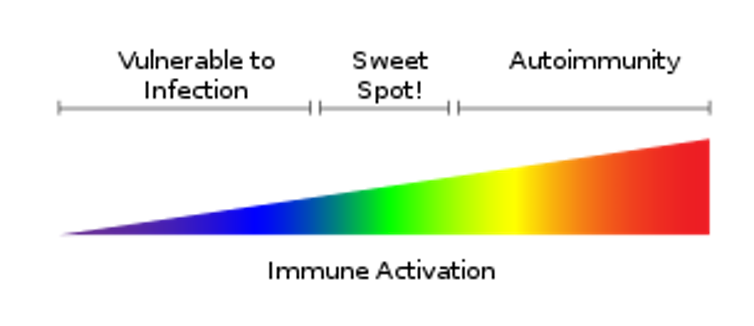
Todos os dias, o seu sistema imune realiza um delicado ato de malabarismo, defendendo você de milhares de patógenos que causam doenças, ao mesmo tempo em que poupa as células saudáveis do seu corpo. Esse equilíbrio cuidadoso é tão perfeito que a maioria das pessoas não pensa nele até que algo dê errado.
Doenças autoimunes, como diabetes tipo 1, lúpus e artrite reumatoide, são lembranças gritantes do que acontece quando o sistema imune confunde suas próprias células com ameaças que precisam ser atacadas. Mas como o sistema imune distingue entre “próprio” e “estranho”?
O Prêmio Nobel de Fisiologia ou Medicina de 2025 homenageia três cientistas – Shimon Sakaguchi, Mary Brunkow e Fred Ramsdell — cujas descobertas inovadoras revelaram como o sistema imune mantém esse delicado equilíbrio. Seu trabalho sobre dois componentes chave da tolerância imune – células T reguladoras e o gene FOXP3 – transformou a forma como pesquisadores como eu entendem o sistema imune, abrindo novos caminhos para o tratamento de doenças autoimunes e câncer.
Como funciona a tolerância imune
Embora o sistema imune seja projetado para reconhecer e eliminar invasores estranhos, como vírus e bactérias, ele também deve evitar atacar os próprios tecidos do corpo. Esse conceito é chamado de autotolerância.
Durante décadas, os cientistas pensaram que a autotolerância era estabelecida principalmente nas partes do corpo que produzem células imunes, como o timo para as células T e a medula óssea para as células B. Nesses locais, as células imunes recém-criadas que atacam o “eu” são eliminadas durante o desenvolvimento por meio de um processo chamado tolerância central.
No entanto, algumas dessas células imunes autorreativas escapam desse processo de eliminação e são liberadas no resto do corpo. A descoberta de Sakaguchi em 1995 de uma nova classe de células imunes, chamadas células T reguladoras, ou “Tregs”, revelou outra camada de proteção: a tolerância periférica. Essas células atuam como guardas de segurança do sistema imune, patrulhando o corpo e suprimindo respostas imunes prejudiciais que poderiam levar a doenças autoimunes.
Enquanto Sakaguchi identificou as células, Brunkow e Ramsdell descobriram em 2001 a chave molecular que as controla. Eles descobriram que mutações em um gene chamado FOXP3 causavam uma doença autoimune fatal em camundongos. Mais tarde, eles mostraram que mutações semelhantes em humanos levam à desregulação imune e a uma doença autoimune rara e grave chamada síndrome IPEX, abreviação de “síndrome de imunodesregulação, polienocrinopatia, enteropatia ligada ao cromossomo X”. Essa doença resulta da ausência ou do mau funcionamento das células T reguladoras.
Em 2003, Sakaguchi confirmou que o FOXP3 é essencial para o desenvolvimento das células T reguladoras. O FOXP3 codifica um tipo de proteína chamada fator de transcrição, o que significa que ajuda a ativar os genes necessários para o desenvolvimento e funcionamento das células T reguladoras. Sem essa proteína, essas células não se formam ou não conseguem suprimir respostas imunes prejudiciais.
Usando o sistema imune na medicina
As células T reguladoras podem ser heroínas ou vilãs, dependendo do contexto. Quando as células T reguladoras não funcionam, isso pode levar a doenças. Uma falha na tolerância imune pode resultar em doenças autoimunes, nas quais o sistema imune ataca tecidos saudáveis. Por outro lado, no câncer, as células T reguladoras podem ser muito eficazes na supressão das respostas imunes que, de outra forma, poderiam destruir os tumores.
A compreensão de como o FOXP3 e as células T reguladoras funcionam deu início a uma nova era nas imunoterapias que aproveitam o sistema imune para tratar doenças autoimunes e câncer. Para doenças autoimunes como artrite reumatoide e diabetes tipo 1, os pesquisadores estão explorando maneiras de aumentar a função das Tregs. Para o câncer, o objetivo é inibir as Tregs, permitindo que o sistema imune ataque os tumores de forma mais agressiva.
Além do tratamento de doenças, essa pesquisa pode melhorar o transplante de órgãos, em que a tolerância imune é crucial para evitar a rejeição. Os cientistas estão explorando como projetar ou expandir as Tregs para ajudar o corpo a aceitar tecidos transplantados a longo prazo.
Continuar a desvendar os segredos da regulação imune pode ajudar a levar a um futuro em que o sistema imune possa ser ajustado com precisão como um termostato – seja para diminuí-lo na autoimunidade ou aumentá-lo contra o câncer.
O Prêmio Nobel de 2025 nos lembra que a ciência, em sua melhor forma, não apenas explica o mundo – ela muda vidas.